اسپکتروفتومتر، دستگاهی است که بر اساس جذب نور کار میکند و در دو نوع تک پرتو و دو پرتو ساخته میشود.
ویدئو کار با دستگاه اسپکتروفتومتر
اگر شما از آن دسته افرادی هستید که به تماشای ویدئو نسبت به مطالعه مقاله بیشتر علاقه دارید، پیشنهاد میکنیم تا ویدئو طیف گیری با اسپکتروفتومتر لِنا را مشاهده کنید. لازم به ذکر است تا بیان کنیم که این ویدئو محتویات یکسانی با مقاله ندارد. هم چنان پیشنهاد ما این است که تا انتها مقاله را مطالعه کنید.
اسپکتروفتومتر تک پرتو
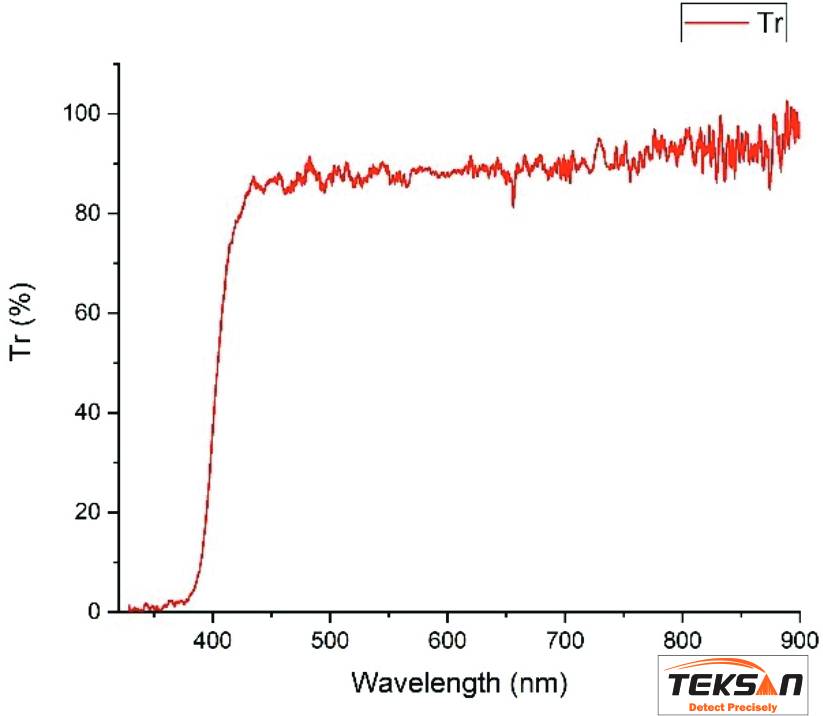
در اسپکتروفتومتر تک پرتو از یک کووت برای تجزیه و تحلیل استفاده میشود. مکانیزم سیستم تک پرتو به این صورت است که پرتو نور ابتدا از داخل یک محلول مرجع (بلانک) عبور میکند. محلول بلانک یا مرجع، محلولی است که همه ترکیبات به جز آنالیت مورد نظر را شامل میشود. به عنوان مثال در آزمایشی، غلظت پروتئین اندازهگیری میشود. برای این منظور، پروتئین باید در حلالی (مانند آب و …) حل شود. این حلال نمونهای از محلول بلانک است. از محلول بلانک برای کالیبره کردن اسپکتروفتومتر نیز استفاده میشود. این امکان را به شما میدهد تا قبل از هرگونه اندازه گیری، اسپکتروفتومتر را روی صفر تنظیم کنید. بعد از اندازهگیری محلول مرجع نوبت به اندازهگیری محلول نمونه میرسد. نمونه با رفرنس جابهجا میشود و این بار نور UV-VIS از داخل نمونه عبور میکند. مقدار جذب حاصل از اندازهگیری محلول مرجع از مقدار جذب نمونه کم میشود تا اثرات تولید شده توسط حلال و کووت از بین برود. به این ترتیب طیف جذبی (عبوری) نمونه بر اساس تابعی از طول موج به دست میآید. این نوع اسپکتروفتومتر برای کاربردهایی در محدوده طول موج ۱۱۰۰-۱۹۰ نانومتر مناسب است. انواع مختلفی از نمونه ها از جمله محلولهای رنگی، اسید نوکلئیک، پروتئینها و تعدادی مولکول آلی اغلب در این ناحیه مورد تجزیه و تحلیل قرار میگیرند.

اسپکتروفتومتر تک پرتو، بسته به نوع آزمایش و کاربرد شما دارای مزایا و معایبی است که در زیر بیان شده است.
مزایا
- از محاسن این سیستم میتوان به سادگی، کوچکی و ارزانی آن اشاره کرد.
- برای کاربردهای عمومی بسیار مقرون به صرفه و کارآمد است.
- تعداد اجزای نوری کمتری برای انتقال نور به کار رفته است که سبب کاهش نویز می شود.
معایب
- نمونه و مرجع در یک زمان مورد تجزیه و تحلیل قرار نمیگیرند. این سبب میشود تا زمان طیفگیری کمی افزایش یابد.
اسپکتروفتومتر دو پرتو
در اسپکتروفتومتر دو پرتو، از دو کووت برای تجزیه و تحلیل استفاده می شود. پرتو نور توسط Beam splitter به دو باریکه نوری تقسیم میشود. این دو باریکه نور همزمان از نمونه و محول مرجع عبور میکند و مقدار جذب محاسبه میشود.

مزایا
- نمونه و مرجع به طور همزمان مورد تجزیه و تحلیل قرار میگیرند. همین امر موجب پایداری سیستم طیف گیری میشود. در واقع اسپکتروفتومتر دو پرتو برای جبران تغییرات شدت منبع نور، بین اندازهگیری نمونه و مرجع ساخته شده است.
- نسبت توان مرجع و نمونه مرتبا به دست میآید.
- سرعت اسکن در طیف وسیعی از طول موج، سریع است.
معایب
- نسبت به اسپکترفتومترهای تک پرتو گرانتر است.
عوامل تاثیرگذار در آزمایش اسپکتروفتومتری
کار با دستگاههای اسپکتروفتومتر لِنا بسیار آسان است. برای انجام آزمایشها با استفاده از طیفسنج تک پرتو، کافی است ابتدا محلول مرجع را داخل دستگاه قرار دهید و طیفگیری را آغاز کنید. مرتبه دوم محلول sample را در محل قرارگیری نمونه بگذارید و دوباره طیفگیری نمایید. با توجه به نوع آزمایشی که در نظر گرفتید میزان جذب یا عبور به دست میآید. استفاده از اسپکتروفتومتر دو پرتو، انجام آزمایش را برای کاربر آسانتر میکند. برای به دست آوردن طیف جذبی (عبوری)، محلول مرجع و نمونه همزمان در دستگاه قرار میگیرند و طیفگیری انجام میشود.
طیف جذبی، تحت تأثیر عواملی از جمله حلال و انتقالات الکترونی قرار میگیرد که هر یک از آنها جداگانه بررسی شده است.
تأثیر حلال بر طیف جذب
خوب است بدانیم که حلالی که آنالیت در آن حل میشود، ممکن است با طیف جذبی آنالیت شما تداخل داشته باشد. حلال، ماهیت قطبی و غیر قطبی دارد. مثلا هیدروکربنهای اشباع شده، حلالهای غیر قطبی هستند و اگر کاملا خالص باشند، با مولکولهای ماده حل شونده تداخلی ندارند. اما حلالهایی مانند آب یا الکلها با توجه به قطبی بودن آنها، اوربیتال مولکولهای آنالیت را در حالت پایه و برانگیخته تغییر میدهند. حلالها (چه قطبی و چه غیر قطبی) در طیف جذب مواد نقش برجستهای دارند. بنابراین حلال باید دارای دو ویژگی باشد:
- نباید با آنالیت برهمکنش داشته باشد.
- نباید در طیف جذب آنالیت تداخل ایجاد کند.
حلال بر اساس خواص جذبی باید در بازه طول موجی مورد نظر انتخاب شود. همچنین باید مناسب ماده و شرایط آزمایش باشد. در جدول ۱ لیست حلالهای رایج و حد پایین بازه طول موجی مفید آنها آورده شده است. هنگام استفاده از حلالهای فرار همچون استون یا سیکلوهگزان، از بسته بودن درب ظرف نمونه اطمینان حاصل کنید. تبخیر حلال میتواند سبب تغییر غلظت محلول یا جریانهای همرفتی شده و دقت اندازهگیری را کاهش دهد. همچنین هنگام استفاده از آب به عنوان حلال توصیه میشود از آب دیونیزه یا آب دیونیزه HPLC استفاده نمایید تا از میزان جذب ناخواسته ناشی از ناخالصیهای آب کاسته شود.
| حلال | حد پایین بازه عبور |
| اسید سولفریک (۹۶٪) آب استونیتریل | ۱۹۵ – ۱۸۰ نانومتر |
| سیکلوپنتان -nهگزان گلیسرول ۴٬۲٬۲-تریمتیلپنتان متانول | ۲۱۰ – ۲۰۰ نانومتر |
| -nبوتیل الکل ایزوپروپیل الکل سیکلوهگزان اتیل اتر | ۲۲۰ – ۲۱۰ نانومتر |
| کلروفرم اتیل استات متیل فرمات | ۲۶۰ – ۲۴۵ نانومتر |
| تتراکلراید کربن دیمتیل سولفوکسید دیمتیل فرمآمید استیک اسید | ۲۷۵ – ۲۶۵ نانومتر |
| بنزن تولوئن متا-زایلین | ۲۹۰ – ۲۸۰ نانومتر |
| پیریدین استون کربن دیسولفید | بالای ۳۰۰ نانومتر |
تأثیر انتقالات الکترونی بر طیف جذبی
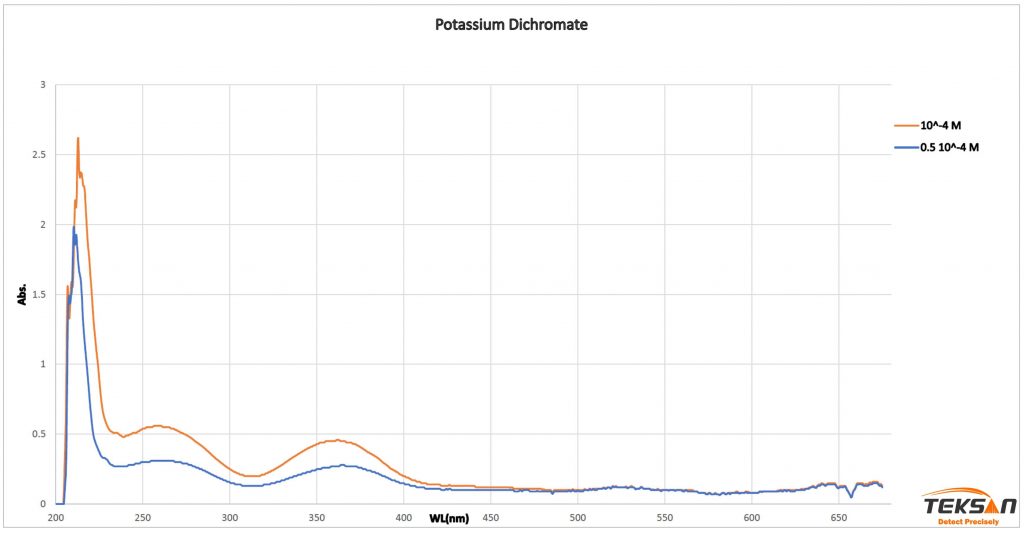
میزان نور جذب شده، مستقیما با مقدار آنالیت موجود در محلول متناسب است. با افزایش غلظت آنالیت، جذب نور نیز به صورت خطی افزایش مییابد. ولی انتقال نور از داخل نمونه به صورت تصاعدی کاهش مییابد و خطی نیست. در ناحیه مرئی-فرابنفش، جذب به ساختار الکترونی گونههای جذب کنننده نور مانند اتمها، مولکولها و یونها بستگی دارد.
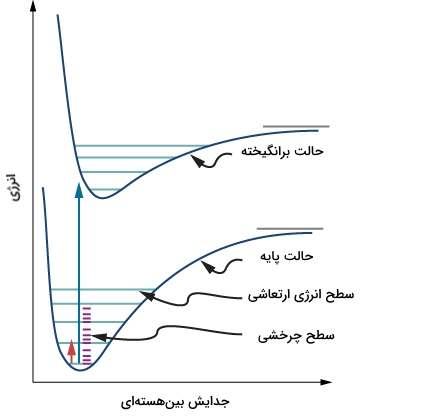
همان طور که در شکل ۴ نشان داده شده است، یک سطح انرژی الکترونی از سطوح انرژی ارتعاشی و یک سطح انرژی ارتعاشی از چندین سطوح انرژی چرخشی (دورانی) تشکیل شده است. هنگامی که یک فوتون با یک مولکول وارد برهمکنش میشود، اگر انرژی فوتون به اندازه اختلاف انرژی ترازهای الکترونی در آن مولکول باشد، آنگاه الکترون تحریک شده و از تراز پایه به یک تراز برانگیخته الکترونی گذار میکند. مقدار تابش جذب شده توسط آنالیت، به منظور به دست آوردن طیف به عنوان تابعی از طول موج اندازهگیری میشود. بنابراین، طیف UV-VIS، یک طرحی از طول موج در برابر شدت است.
همان طور که گفته شد، جذب نور در مولکولها توسط الکترونها صورت میگیرد. الکترونها، فوتونهای نور را جذب کرده و به سطح انرژی بالاتری گذار میکنند. الکترونهای موجود در مولکولها را میتوان به سه دسته تقسیم کرد:
الکترونهای نوع σ
این الکترونها در ساخت پیوند یگانه کووالانسی نقش دارند و برای تحریک آنها انرژی زیادی مورد نیاز است.
الکترونهای نوع π
الکترونهای نوع π در ایجاد پیوند دوگانه یا سه گانه نقش دارند و برای تحریک آنها انرژی نسبتا کمی لازم است.
الکترونهای نوع n
این نوع الکترونها در ایجاد پیوند کووالانسی شرکت نداشته و به صورت آزاد در اطراف اتم قرار میگیرند. این الکترونها به الکترونهای غیر پیوندی نیز شهرت دارند و در مقایسه با الکترونهای نوع π و σ به انرژی تحریک کمتری نیاز دارند.
علاوه بر ماهیت حلال، حالت انتقال الکترونی نیز بر طیف جذب آنالیت تأثیر میگذارد. میان چهار نوع انتقال الکترونی (*π→π*، n→σ*، n→π و *σ→σ)، انتقالهای الکترونی *n→π و *π→π بر طیف جذب آنالیت تأثیر میگذارند (شکل ۵).
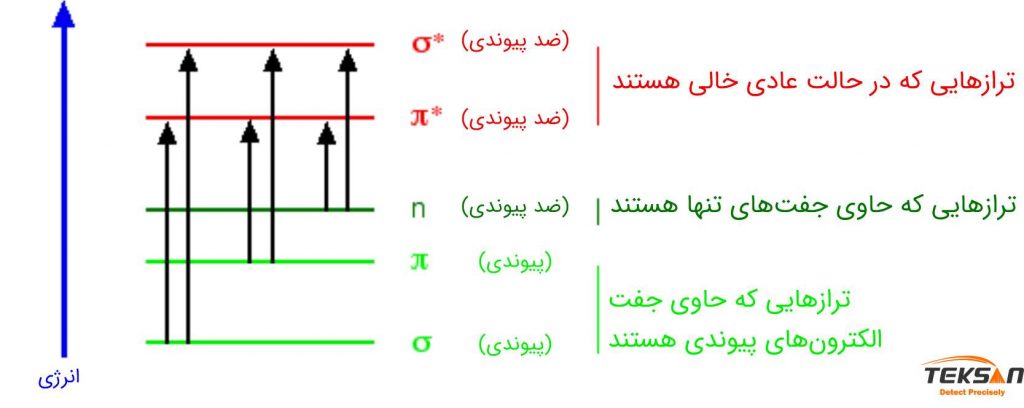
تأثیر انتقال الکترونی *π→π بر طیف جذب
در انتقال *π→π، برهمکنش دو قطبی-دو قطبی با حلال باعث کاهش انرژی الکترونها در حالت برانگیخته در مقایسه با حالت پایه میشود. در حالی که حالت برانگیخته در مقایسه با حالت پایه، قطبش بیشتری نشان میدهد. بنابراین حلالهای قطبی، انرژی گذار الکترونی *π→π را کاهش میدهند.
تأثیر انتقال الکترونی *n→π بر طیف جذب
در انتقال *n→π، درحلالهای قطبی با پیوندهای هیدروژنی، مولکولها در حالت پایه، قطبیتر از حالت برانگیخته هستند. به همین دلیل در حلالهای قطبی، انرژی انتقال الکترونی افزایش مییابد.
تا این قسمت تأثیر حلال و انتقالات الکترونی بر طیف جذب را بررسی کردیم. البته برای داشتن طیف مطلوب باید به چند پارامتر ضروری دیگر نیز توجه کنیم. یکی از این پارامترها انتخاب صحیح جنس کووت است. موضوع دیگر این است که قبل از شروع طیفگیری نکاتی را باید رعایت کنیم. به همین علت، برای شفافتر شدن موضوعات بیان شده، دو بخش بعدی را به این نکات اختصاص دادهایم.
انتخاب کووت
برای به دست آوردن طیف جذبی مطلوب، انتخاب کووت نیز از اهمیت ویژهای برخوردار است. کووتها در اشکال مختلفی در دسترس هستند و برای نگهداری نمونه در آنالیز اسپکتروفتومتری طراحی شده اند. کووتها با توجه به شکل، اندازه، جنس، طول مسیر و مشخصات انتقال طول موج مورد نیاز، متفاوت هستند. برخی از کووتها طوری طراحی شدهاند که فقط طول موجهای خاصی را از خود عبور میدهند. مهمترین معیار انتخاب کووتی که برای آزمایشهای اسپکتروفتومتر UV-VIS مناسب باشد، جنس کووت است. کووت از مواد مختلفی تهیه میشود که چهار ماده مرسوم آن عبارتاند از:
- کووت شیشهای نوری یا پیرکس
- کووت کوارتز UV
- کووت کوارتز IR
- کووت یاقوت کبود
هر یک از این کووتها دارای معایب و مزایایی هستند.
کووتهای پیرکس، برای محدوده مرئی مناسب هستند. دامنه طول موجی ۳۴۰ تا ۲۵۰۰ نانومتر را از خود عبور میدهند و از نظر قیمت این نوع کووتها بسیار مقرون به صرفه هستند.
کووت کوارتز UV، یک پله بالاتر از کووت شیشهای نوری است. نسبت به نوع پیرکس گرانتر هستند اما بازه وسیعتری از طول موجها (۱۹۰-۲۵۰۰ نانومتر) را از خود عبور میدهند و برای انجام آزمایشهایی در محدوده فرابنفش به کار میروند.
کووت کوارتز IR، دارای دامنه انتقالی در محدوده طول موجی 3500-220 نانومتر است. بنابراین اشعه فرابنفش، نور مرئی و اشعه فروسرخ را از خود عبور میدهد.
یاقوت کبود، ماده بسیار سختی است. به طوری که امکان آسیب دیدگی آن بسیار کم است. کووت یاقوت کبود محدوده طول موجی ۲۵۰ تا ۲۵۰۰ نانومتر را عبور میدهد ولی نسبت به سایر کووتها گران قیمتتر است.
| جنس کووت | محدوده انتقال | قیمت |
| شیشهای نوری یا پیرکس | ۳۴۰-۲۵۰۰ نانومتر | $ |
| کوارتز UV | ۱۹۰-۲۵۰۰ نانومتر | $$ |
| کوارتز IR | ۲۲۰-۲۵۰۰ نانومتر | $$$ |
| یاقوت کبود | ۲۵۰-۲۵۰۰ نانومتر | $$$$ |
نکات مهم قبل از طیف گیری
برای به دست آوردن نتیجه بهتر، به نکات زیر توجه کنید و قبل از انجام هرگونه آزمایش، نمونه را برای اندازهگیریها آماده کنید.
- پیش از شروع طیفگیری و قبل از استفاده، ظروف نمونه (مانند کووت و …) باید سه الی پنج مرتبه با حلال مورد نظر شستشو داده شوند. قرار دادن ظروف به صورت وارونه بر روی یک دستمال جاذب، به تخلیه ظرف از باقیمانده حلال کمک میکند. این فرایند اثر آلایندههای باقی مانده از آزمایشهای قبلی را کاهش میدهد.
- نمونههایی که حاوی ذرات کلوییدی معلق، گرد و غبار یا دیگر مواد ذرهای هستند باید فیلتر یا سانتریفیوژ شوند و یا اجازه تهنشین شدن به این ذرات داده شود. در غیر این صورت برآیند اتلاف ناشی از پراکندگی نور و یا بازتاب در طیف عبوری، اطلاعات طیفی مربوط به ماده مورد آزمایش را مختل میکند.
- هنگامی که یک ظرف جدید را با نمونه پر میکنید، حبابهای هوا به دیوارههای ظرف میچسبند و طیفگیری را مختل میکنند. برای جلوگیری از تشکیل حبابهای هوا، ظروف را با مایع پاک کننده و غیر فعالساز بشویید.
- محلول درون ظرف را به صورت همگن مخلوط کنید.
- حتما ظروف نمونه و مرجع از یک جنس انتخاب شوند.
- از حلالهای مناسب استفاده کنید.
روش اندازهگیری غلظت نمونه
منحنی استاندارد
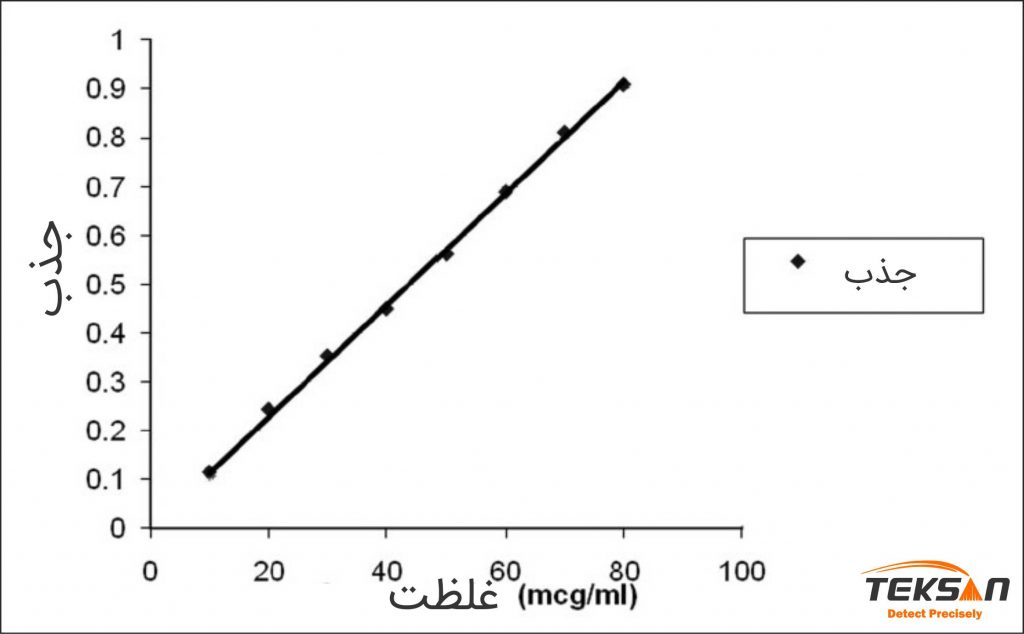
طبق قانون بیر-لامبرت در شرایط ایدهآل، غلظت ماده و میزان جذب آن به صورت خطی با هم متناسباند. در واقع هرچه غلظت یک محلول بیشتر باشد، نور بیشتری جذب میشود. با استفاده از اسپکتروفتومتر علاوه بر میزان جذب (عبور) نور، میتوانید غلظت یک محلول را نیز اندازهگیری کرد. برای این منظور از منحنی استاندارد استفاده میشود. بسیاری از منحنیهای استاندارد خطی هستند و با استفاده از معادله y=mx+b ، میتوان غلظت محلول را به دست آورد. در این معادله m شیب و b عرض از مبدا است.
برای تعیین غلظت مجهول یک نمونه، از همان نمونه در غلظتهای مختلف تهیه میشود و میزان جذب آنها (هم غلظت مجهول و هم سایر نمونهها) در یک طول موج مشخص اندازهگیری میگردد. برای یک منحنی استاندارد خوب حداقل ۵ غلظت، مورد نیاز است. سپس با استفاده از دادههای به دست آمده یک منحنی استاندارد رسم میشود. همان طور که در بالا ذکر شد، این نمودار، یک منحنی خطی است که شیب و عرض از مبدأ آن قابل محاسبه است. غلظت مجهول با در دست داشتن شیب، میزان جذب و عرض از مبدأ به دست میآید. آموزش نحوه رسم نمودار اسپکتروفتومتری در اکسل به همراه ویدئو آن برای شما عزیزان قرار داده شده است.
برای این که بیشتر با نحوه کار با اسپکتروفتومتر لِنا آشنا شوید، میتوانید در کارگاههای طیف سنجی شرکت تکسان شرکت کنید. هم چنین میتوانید جهت دریافت مشاوره رایگان با کارشناسان ما تماس بگیرید.
جمعبندی
اسپکتروفتومتر دستگاهی است که شدت نور را به عنوان تابعی از طول موج اندازهگیری میکند و در دو نوع تک پرتو و دو پرتو ساخته میشود. در نوع تک پرتو از یک کووت برای اندازهگیری استفاده میشود. یعنی یک بار نور از محلول بلانک عبور میکند. سپس به جای محلول بلانک، محلول نمونه قرار میگیرد و این بار طیفگیری از نمونه انجام میگیرد. با مقایسه شدت نور عبوری از محلول بلانک و محلول نمونه، طیف جذبی (عبوری) به دست میآید. در نوع دو پرتو، نور به دو باریکه تقسیم شده و همزمان از نمونه و محلول مرجع عبور میکند. هر دو دستگاه با توجه به نوع عملکردشان، دارای معایب و مزایایی هستند. کار با طیفسنج UV-VIS بسیار آسان است. اما باید به عواملی که بر طیف جذب (حلال و انتقالات الکترونی) تأثیر میگذارند توجه داشت. همچنین باید دستورالعملهای قبل از آزمایش، به منظور بهبود نتایج، انجام گیرد.
در مطالب بعدی به طور کامل به نحوه انجام آزمایش با اسپکتروفتومتر لِنا خواهیم پرداخت. بنابراین شبکههای اجتماعی ما را دنبال کنید تا از مقالات و ویدئوهای جذاب ما مطلع شوید.
منابع
- https://zaya.io/6fat0
- https://zaya.io/rtpcz
- https://zaya.io/k701x
- https://zaya.io/fepbl
- https://zaya.io/vu305
- https://zaya.io/qgs4w
- https://zaya.io/7u54q
- https://zaya.io/0wt44
- https://zaya.io/pp54l