تکنیک اسپکتروفتومتری جذبی میتواند هم به عنوان یک ابزار کیفی برای شناسایی مواد، و هم به عنوان ابزاری کمی برای اندازه گیری غلظت ماده در یک حلال استفاده شود. در برخی موقعیتها، برای اندازهگیری جذب مطلق یا ضریب میرایی ماده ناشناخته نیز کاربرد دارد. در یک آنالیز کمی محاسبات از اندازهگیری محلولهای استاندارد و استفاده از آنها برای تعیین غلظت محلولهایی با غلظت مجهول استفاده میشود. در هر صورت، آنالیز کمی استفادهای از قانون بیر-لامبرت است.
تعریف مرجع (Reference or Blank)
یک آزمایش جذب شامل اندازهگیری شدت یک پرتو نور موازی شده قبل و بعد از حضور نمونه است. برای مایعات، نمونه در یک محفظه شیشهای به نام کووت (Cuvette) نگه داشته میشود.

برای انجام یک آنالیز کمی از قانون بیر-لامبرت بهره خواهیم گرفت. قانون بیر- لامبرت ارتباط بین نور جذب شده در ماده را با غلظت و طول مسیر نور در ماده بیان میکند.
I = I۰ exp -(αcl)
در این رابطه I۰ شدت قبل از ورود به ماده، α ضریب جذب، c غلظت ماده و l طول پیمایش نور درون ماده است. صورت لگاریتمی این قانون بیشتر مرسوم است:
Aλ = – log (I / I۰ ) = αcl
Aλ = ABS = αcl
پارامتر Aλ یا ABS را جذب ماده مینامند و همان طور که مشاهده میشود، نسبت خطی با غلظت ماده دارد. از این رابطه خطی برای رسم نمودار کالیبراسیون و یافتن غلظت مواد استفاده میشود.
باید توجه داشته باشید که در قانون بیر-لامبرت I۰ شدت نور قبل از ورود به نمونه و I شدت نور بعد از عبور از نمونه است. اما در یک آزمایش جذب واقعی، جذب نور توسط شیشه نگه دارنده و بازتابهای متوالی از سطوح نگه دارنده شیشه نیز قسمتی از نور را تلف خواهد کرد. برای در نظر گرفتن این اثرات، I۰ به عنوان شدت نور عبوری از کوت شیشهای خالی یا کوت حاوی حلال (نمونه مرجع) در نظر گرفته میشود. I نیز شدت عبور کرده از کوت حاوی نمونه است.
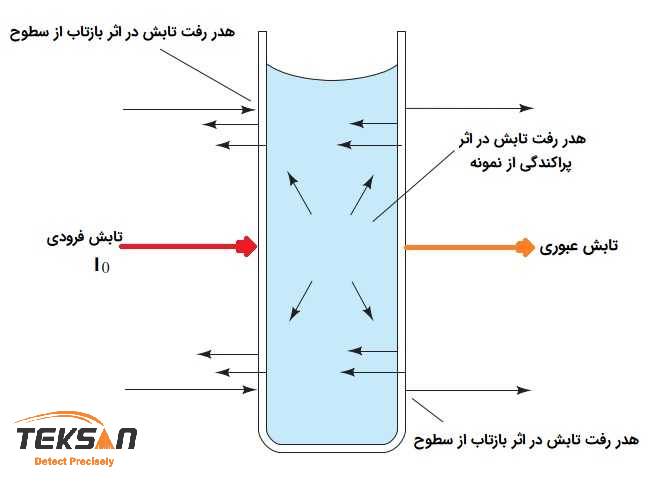
ABS = – log (I / I۰ ) ≅ – log (Isample / Iblank )
چند نکته را در مورد این معادلات در نظر داشته باشید:
- شدت اولیه بیشتر از نوری است که از نمونه عبور میکند. زیرا مقداری از انرژی توسط مولکولهای نمونه جذب می شود.
- یکای اندازهگیری (دیمانسیون) ضریب جذب در قانون بیر-لامبرت Lit/ mol. cm است، اگر غلظت بر حسب Mol/ Lit و طول نمونه بر حسب cm باشد.
- یکای اندازهگیری (دیمانسیون) ضریب جذب در قانون بیر-لامبرت Lit/gr.cm است، اگر غلظت بر حسب g/Lit و طول نمونه بر حسب cm باشد.
- اگر به جای جذب (ABS)، دستگاه درصد عبور (T%) را گزارش کند، با رابطهی زیر میتوان ABS را محاسبه نمود:
ABS = 2 – log (%T)
آنالیز کمی با تکنیک اسپکتروفتومتری و دستگاه اسپکتروفتومتر
برای یافتن غلظت مجهول از یک ماده ابتدا باید نمودار کالیبراسیون را با توجه به غلظتهای معلوم به دست آوریم. برای این کار ابتدا غلظتهای مشخصی از ماده را تهیه میکنیم و پس از آن با استفاده از یکی از نمونههای استاندارد طیف جذب در کل ناحیه طیفی را مشخص میکنیم. این کار برای پیدا کردن پیکهای جذب احتمالی ماده انجام میشود.
میزان جذب (ABS) در یکی از پیکهای جذبی ماده باید اندازهگیری شود. چون در این حالت خطاهای ناشی از غیرخطی بودن نمودار کالیبراسیون به کمترین حالت خود نسبت به طول موج های دیگر می رسد.
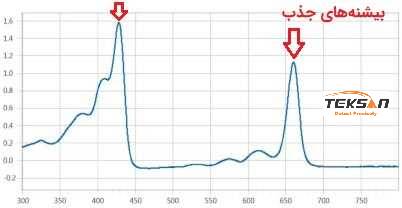
اکنون میزان جذب برای همه نمونههای استاندارد در طولموج مشخص شده اندازهگیری شده و بر مبنای آن نمودار کالیبراسیون رسم میگردد.
| غلظت (gr//Lit) | ABS |
| ۰.۱۱ | ۰.۲۹ |
| ۰.۱۹ | ۰.۸ |
| ۰.۴۲ | ۱.۱۵ |
| ۰.۷۸ | ۲.۵ |
| ۱.۶۱ | ۴.۷۵ |
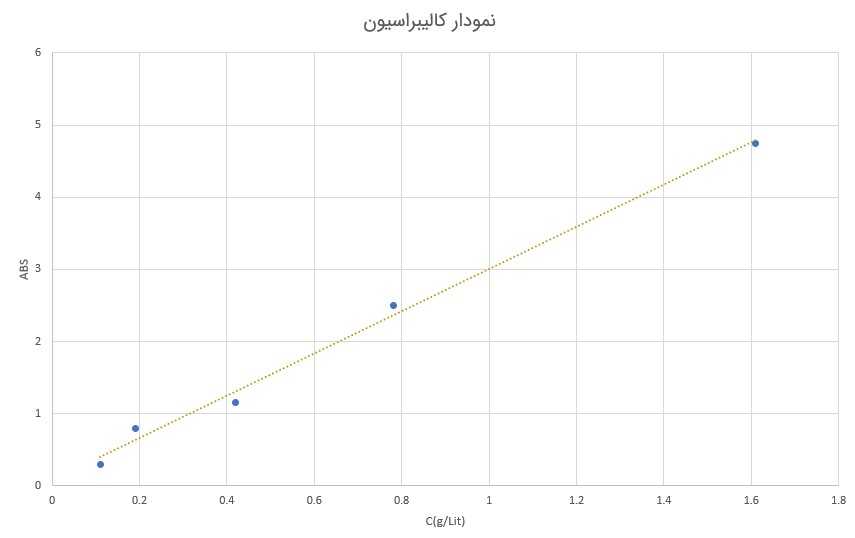
پس از رسم نمودار کالیبراسیون و به دست آوردن بهترین تابع خطی برازش شده به نقاط، اکنون میتوان غلظت نمونه مجهول را با اندازهگیری ABS آن و قرار دادن در معادله پیدا کرد.
به طورخلاصه طیف سنجی کمی با تکنیک UV-Vis مزایای زیر رادارد:
- کاربرد گسترده ای در ترکیبات آلی و غیر آلی
- تجزیه و تحلیل محلول های بسیار رقیق (کمتر از یک صدم مولار)
- حساسیت های خوب معمولاً در حد ۶-۱۰-۴-۱۰ مولار
- دقت خوب و سرعت بالا در مقایسه با سایر روشهای کمی
- سهولت راهاندازی و سهولت اندازه گیری و به دست آوردن دادهها
استفاده از اسپکتروفتومتر برای آنالیز کمی در حوزههای تحقیقاتی و صنعتی زیادی و برای مواد بیشماری مرسوم است. اما پرکاربردترینها را میتوانید در لیست زیر ببینید:
تعین غلظت
- یونهای فلزی به عنوان مثال آهن ، مس ، نیکل در داروسازی
- یونهای غیر آلی، به عنوان مثال نیترات در تصفیه آب
- تقاضای اکسیژن شیمیایی (COD) در F&B و آبکاری
تجزیه و تحلیل تغییر غلظت با زمان
- سینتیک آنزیم: تعیین میزان تجزیه در دارو
- کاتالیز Glucose oxidase – اکسیداسیون β-D-گلوکز توسط اکسیژن (۷۲۵ و ۴۱۵ نانومتر)
- اکسیداسیون و کاهش نوکلئوتیدهای pyridine
- NAD + / NADH ، ۳۴۰ نانومتر
- نرخ اکسیداسیون کلسترول توسط تجزیه با Cholesterol Oxidase (500 نانومتر)
- تست GPO colorimetric kinetic برای تری گلیسیرید (۵۲۰ نانومتر)
پارامترهای فیزیکی-شیمیایی
- ثابت تفکیک اسید
- ثابت Complex formation
- ضریب توزیع پارتیشن
- تست انحلال
آنالیز کیفی به وسیله اسپکتروفتومتری
ابتدا برای گرفتن طیف مناسب از نمونه و شناسایی آن باید از یک حلال مناسب جهت طیف سنجی استفاده کنیم. همه حلالهای شفاف برای ناحیه مرئی مناسب هستند. اما برای ناحیه فرابنفش و فروسرخ باید از حلالهای مناسب استفاده شود. حلالهای مرسوم با کمترین طول موج قابل استفاده در در جدول زیر لیست شدهاند:
| حلال | کمترین طول موج مجاز (nm) |
| water | ۱۹۰ |
| ethanol | ۲۱۰ |
| n-hexane | ۱۹۵ |
| cyclohexane | ۲۱۰ |
| benzene | ۲۸۰ |
| diethyl ether | ۲۱۰ |
| acetone | ۳۱۰ |
| acetonitrile | ۱۹۵ |
| carbon tetrachloride | ۲۶۵ |
| methylene chloride | ۲۳۵ |
| chloroform | ۲۴۵ |
آیا میتوان با روش اسپکتروفتومتری مواد را شناسایی نمود؟ پاسخ به بخشی از سیستم مورد بررسی شما بستگی دارد. ابتدا باید در مورد مواد آلی گفت:
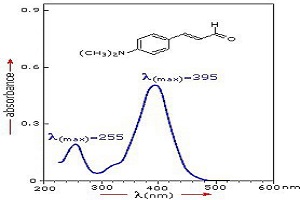
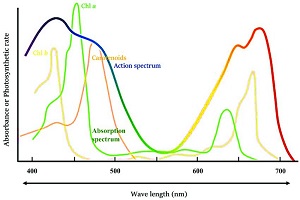
مولکولهای آلی جذب کننده ماورابنفش، معمولاً در ساختار خود شامل انتقالهای *n- π و *π- π هستند. از آن جایی که طیفهای جذب UV / VIS معمولاً در دمای اتاق ثبت میشوند، پهن شدگی تصادفی منجر به از بین رفتن تفکیک خطوط تیز گذارها در تمام خطوط جداگانه میشود که مطابق با تحریکات به حالتهای مختلف ارتعاشی و چرخشی یک حالت الکترونیکی مربوط میشوند.
از طرفی، طیف های جذب UV / VIS ترکیبات آلی تفاوت چندانی با یکدیگر ندارند. در حالی که میتوان با استفاده از طیفهایی که در طیف سنجی NMR یا طیف سنجی رامان به دست میآیند، ساختارهای منحصر به فردی را به مولکولها اختصاص داد. طیفهای طیف سنجی UV / VIS جزئیات کافی برای چنین تجزیه و تحلیلی را ندارند. بنابراین، طیف سنجی UV / VIS ابزاری مفید برای تجزیه و تحلیل کیفی ترکیبات آلی نیست.
با این حال، برخی ترکیبات آلی خاص دارای طیف جذب UV / VIS خاصی هستند. اگر طیف یک ترکیب ناشناخته دقیقاً با یک ترکیب شناخته شده مطابقت داشته باشد (به شرطی که هر دو تحت یک شرایط ثبت شده باشند (در یک حلال ، با همان pH و غیره). این یک گواه محکم است که ترکیبات یکسان هستند. با این حال، به دلیل ماهیت عدم اثر انگشتی بودن بسیاری از طیفهای UV / VIS، باید با احتیاط به چنین نتیجهای رسید. استفاده از آشکارساز UV-VIS به عنوان روش تشخیص در کروماتوگرافی مایع کاملا معمول است. در این حالت، برای تأیید انتساب هویت ترکیب میتوان از مطابقت طیفهای یکسان با همسان سازی پیشرفته بین یک معلوم و یک مجهول استفاده کرد.
بسیاری از یونهای فلزها، گذارهایی در ناحیه جذب UV / VIS دارند که متمایز هستند و اکثرا شامل انتقال الکترونی d-d هستند. موقعیت قلهها در طیفها بسته به لیگاند میتواند به میزان قابل توجهی متفاوت باشد. مفهومی به نام سری اسپکتروشیمیایی وجود دارد که میتواند برای پیش بینی تغییرات خاصی که با تنوع لیگاندها مشاهده خواهد شد، در این کاربردها مورد استفاده قرار گیرد. از طیف سنجی UV / VIS میتوان برای تأیید وجود یک نوع فلز خاص در محلول استفاده کرد. برخی از گونههای فلزی نیز دارای فرآیند جذبی هستند که ناشی از یک فرآیند انتقال بار است. در فرآیند انتقال بار، الکترون از حالت HOMO در یک گونه به حالت LUMO در گونه دیگر میرود. در ترکیبهای فلزی، این می تواند شامل انتقال لیگاند به فلز یا انتقال فلز به لیگاند باشد. انتقال لیگاند به فلز متداولتر است و این فرآیند به طور موثر انتقال الکترونی یا واکنش اکسیداسیون داخلی را نشان میدهد. جفتهای خاصی از ترکیبات آلی نیز در محلول فعالیت دارند و از انتقال بار استفاده میکنند. یک جنبه مهم از انتقال بار این است که آنها تمایل دارند که جذب مولار بسیار بالایی داشته باشند.
متغیرهای موثر بر طیف های جذب UV / VIS
چه متغیرهایی بر طیفهای جذب UV / VIS تأثیر میگذارند و هنگام انجام تجزیه و تحلیل کمی و کیفی، باید لحاظ شوند؟
- حلال می تواند تاثیری داشته باشد و باعث شیفتهای bathochromic و hypsochromic شود.
- گونههایی در ماتریس نمونه که ممکن است برهم کنش دو قطبی-دو قطبی مثل پیوندهای هیدروژنی ایجاد کنند، می توانند طیفها را تغییر دهند.
- یونهای فلزی که میتوانند کمپلکسهای دهنده – پذیرنده را تشکیل دهند، میتوانند همین تأثیر را داشته باشند.
- دما میتواند بر روی طیف برخی نمونهها تأثیر بگذارد.
- غلظت الکترولیت نیز می تواند تأثیرگذار باشد.
- پارامتر PH میتواند اثر بارزی در طیف داشته باشد. زیرا طیف اسیدها و بازهای protonated و deprotonated میتوانند تفاوت چشمگیری با یکدیگر داشته باشند.
جمع بندی
تکنیک (UV / VIS) به طور گستردهای در تحقیقات، تولید و کنترل کیفیت برای طبقه بندی و مطالعه مواد استفاده میشود. طیف سنجی UV / VIS براساس جذب نور توسط یک نمونه، بنا شده است. بسته نمونه به میزان نور و طول موج خاصی در نمونه جذب میشود، میتوان از این اطلاعات دادههای ارزشمندی مانند نوع و غلظت نمونه را به دست آورد. علاوه بر این، مقدار نور جذب شده به مقدار نمونه مربوط است و بنابراین تجزیه و تحلیل کمی توسط طیف سنجی نوری امکان پذیر است.
برای کسب اطلاعات بیشتر با ما در تماس باشید.