شیمی علمی است که به جرات میتوان گفت در همه زمینهها از جمله داروسازی، صنایع غذایی، سنتز مواد و غیره کاربرد دارد. به همین دلیل مطالعه این علم از طریق ابزارهای اندازهگیری حائز اهمیت است. اسپکتروفتومتری روشی است که در آن با استفاده از اندازهگیری میزان جذب و یا عبور نور برخی از خواص مواد را مشخصهیابی میکند. بنابراین از این روش در شیمی به طور فراوان استفاده میشود. دستگاهی که برای این روش به کار گرفته میشود اسپکتروفتومتر نامیده میشود.
به وسیله این روش میتوان آنالیز کمی و کیفی انجام داد که در ادامه به توصیف آنها خواهیم پرداخت.
اسپکتروفتومتری برای تجزیه و تحلیل کیفی مواد در شیمی
از روش اسپکتروفتومتری برای تشخیص ساختار ترکیبات آلی و غیر آلی در یک مخلوط استفاده میشود. تجزیه و تحلیل کیفی به دو منظور در آزمایشگاههای شیمی به کار میرود: ۱) تحلیل ساختار ترکیبات آلی و ۲) تشخیص ناخالصیها.
تجزیه و تحلیل کیفی ساختار ترکیبات آلی
طیف سنجی مرئی فرابنفش در تحلیل ساختار ترکیبات آلی و تشخیص اشباع یا عدم اشباع روش کارآمدی است. محل قرارگیری قلهها و ترکیب قلهها، در تشخیص به ما کمک میکند. همچنین وجود یک باند جذبی در طولموج خاص نشان دهنده وجود یک کروموفور خاص در ترکیبات است. علاوه بر این از این روش برای شناسایی conjugated dienes، پلینها (polyenes)، ترکیبات کربونیل اشباع نشده و ترکیبات معطر استفاده میشود.
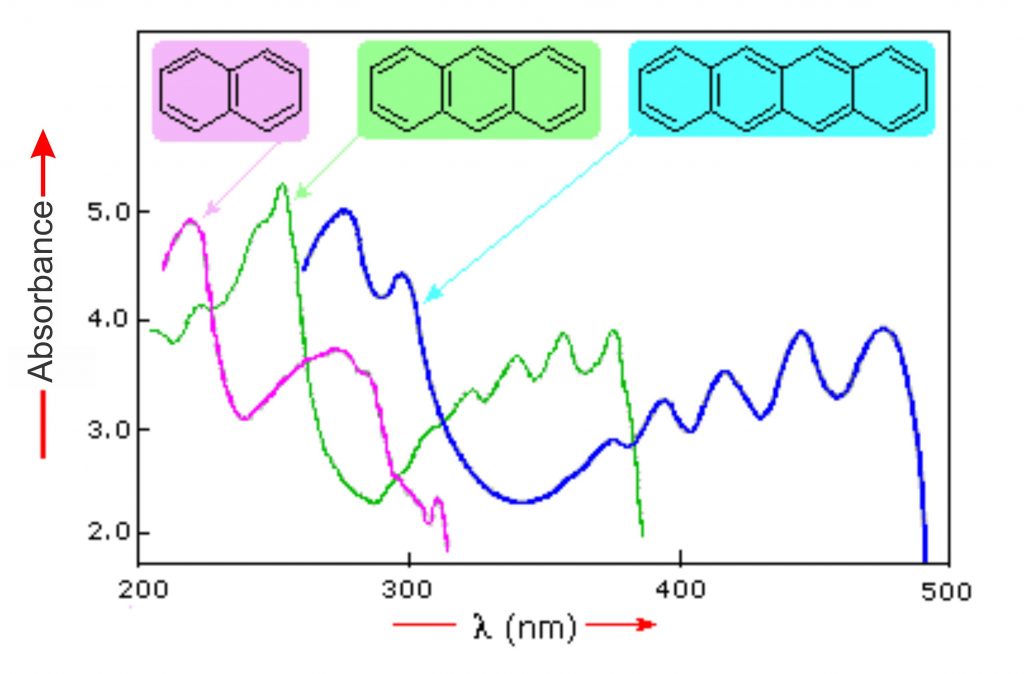
نحوه جذب نور توسط مولکولهای ماده موجب میشود تا هر مادهای نور را در فرکانس یا طولموجهای خاصی جذب کند. همین منجر به تشخیص ترکیبات میشود.
طیف سنجی UV-VIS در تشخیص ناخالصیهای یک ماده
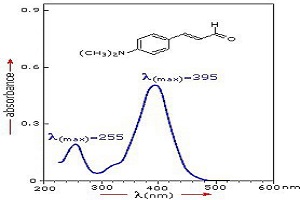
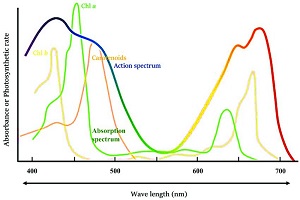
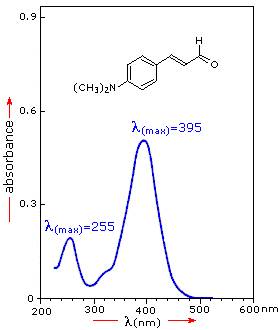
اسپکتروفتومتری مرئی-فرابنفش یکی از بهترین روشها برای تعیین ناخالصیهای موجود در مولکولهای آلی است. این ناخالصیها دارای باند خاصی در طیف جذبی هستند و میتوان با مقایسه طیف جذب استاندارد آن ماده ناخالصیها را تعیین کرد. به عنوان مثال بنزن به عنوان یک ناخالصی رایج در سیکلوهگزان مشاهده میشود و از روی طیف جذبی سیکلوهگزان قابل تشخیص است. بنزن در طولموج ۲۵۵ نانومتر دارای یک باند جذبی است (شکل ۲).
اسپکتروفتومتری برای تجزیه و تحلیل کمی مواد در شیمی
همان طور که پیشتر هم اشاره شد با استفاده از اسپکتروفتومتری میتوان آنالیزها را به صورت کمی نیز انجام داد. منظور از تجزیه و تحلیل کمی، تعیین غلظت ترکیبات، سینتیک شیمیایی و ثابت تفکیک اسیدها و بازها است.
تعیین غلظت ترکیبات
غلظت ترکیبات به روش اسپکتروفتومتری بر اساس قانون بیر-لامبرت تعیین میگردد. طبق این قانون میزان جذب نور برای یک ماده از رابطه زیر قابل محاسبه است:
A= log I۰ / I = – log T= ε l c
در این رابطه A میزان جذب، I۰ شدت نور اولیه، I شدت نور پس از عبور از نمونه، T میزان عبور نور، ε ضریب جذب مولی، l طول مسیر نوری و c غلظت نمونه است. همان طور که از رابطه بیر-لامبرت پیدا است، میزان جذب و غلظت یک ماده رابطه مستقیمی دارند. یعنی هرچه غلظت یک ماده در محلول بیشتر شود میزان جذب آن نیز به صورت خطی افزایش مییابد. معمولا برای تعیین غلظت از نمودار استاندار یا نمودار اسپکتروفتومتری استفاده میشود. به این ترتیب غلظتهای مجهول به دست میآید.
سینتیک شیمیایی (مطالعه واکنشهای شیمیایی)
سینتیک شیمیایی که به عنوان سینتیک واکنش نیز شناخته میشود، شاخهای از علم شیمی است که سرعت واکنشهای شیمیایی را تجزیه و تحلیل میکند. سینتیک شیمیایی شامل بررسی چگونگی تاثیر شرایط تجربی بر سرعت واکنش شیمیایی، ارائه اطلاعات در مورد مکانیسم واکنش، حالتهای گذار و همچنین ساخت مدلهای ریاضی است که میتواند ویژگیهای یک واکنش شیمیایی را نیز توصیف کند.
طیف سنجی UV-VIS برای مطالعه میزان واکنشهای شیمیایی به کار گرفته میشود. در این زمینه اگر واکنش دهنده یا محصول واکنش، تابش را در طولموج خاص جذب کند، میتوان از طیف سنجی برای اندازهگیری جذب به عنوان تابعی از زمان استفاده کرد. به این ترتیب میتوان سرعت واکنش را نیز اندازهگیری کرد. باید توجه داشت که این اندازهگیریها فقط به وسیله اسپکتروفتومتر دو پرتو ممکن است. در واقع میتوان گفت که یکی از اصلیترین تفاوتهای اسپکتروفتومتر تک پرتو و دو پرتو همین نکته است.
برای توضیح بیشتر این مسئله را با ارائه یک مثال توصیف میکنیم. در آزمایشی میخواهیم پروتون را از نیترواتان حذف کنیم. این کار را به کمک یون هیدروکسید انجام میدهیم.
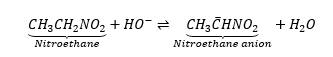
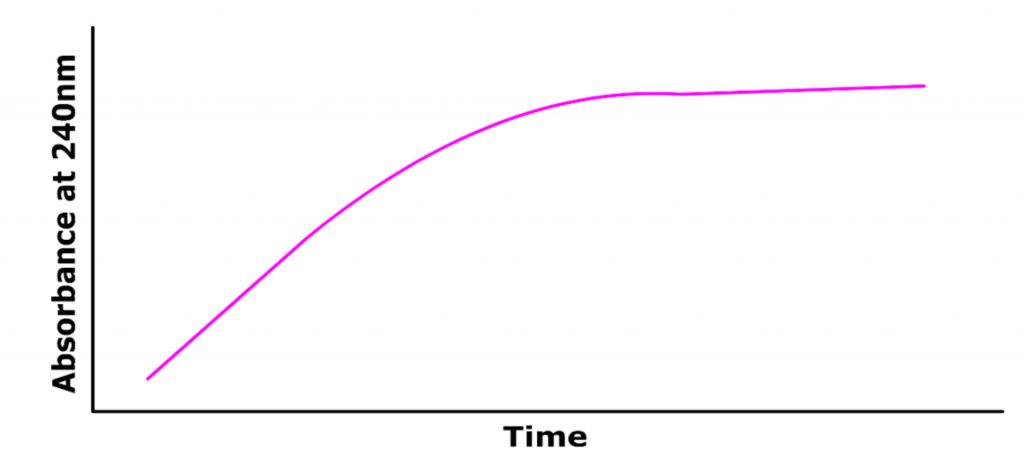
در این مثال آنیون نیترو اتان نور UV را در طولموج ۲۴۰ نانومتر جذب میکند. این درحالی است که سایر واکنش دهندهها یا محصولات جذب قابل توجهی در این طولموج نشان نمیدهند. به منظور اندازهگیری میزان حذف پروتون از نیترواتان، اسپکتروفتومتر UV برای اندازهگیری جذب در ۲۴۰ نانومتر به عنوان تابعی از زمان تنظیم میشود. میزان جذب با گذشت زمان در طولموج ۲۴۰ نانومتر به صورت شکل ۳ تغییر میکند.
یکی از پرکاربردترین تجزیه و تحلیلهای سینتیک شیمیایی، اندازهگیری سرعت طیف سنجی برای مطالعه آنزیمها است. آنزیمها را نمیتوان مستقیما اندازهگیری کرد. اما از روی سرعت واکنشهایی که کاتالیز میکنند، میتوان آنزیمها را مورد مطالعه قرار داد.
ثابت تفکیک اسیدها و بازها
از نمودار طیف جذب اسیدها و بازها میتوان ثابت جذب این ترکیبات را تعیین کرد. به عنوان مثال یون فنوکسید (phenoxide) در طولموج ۲۸۷ دارای بیشترین جذب است. اگر جذب به عنوان تابعی از pH تعیین شود در این صورت ثابت تفکیک را میتوان از معادله هندرسون-هاسلبالچ (Henderson–Hasselbalch) به دست آورد.
اسپکتروفتومتری در مطالعه مجموعههای انتقال بار (charge transfer complexes)
علاوه بر تجزیه و تحلیل کمی و کیفی، آنالیزهای دیگری هم میتواند توسط اسپکتروفتومتری در زمینه شیمی انجام شود. مجموعههای انتقال بار زمانی به وجود میآید که الکترون از مولکولی به مولکول دیگر انتقال یابد.
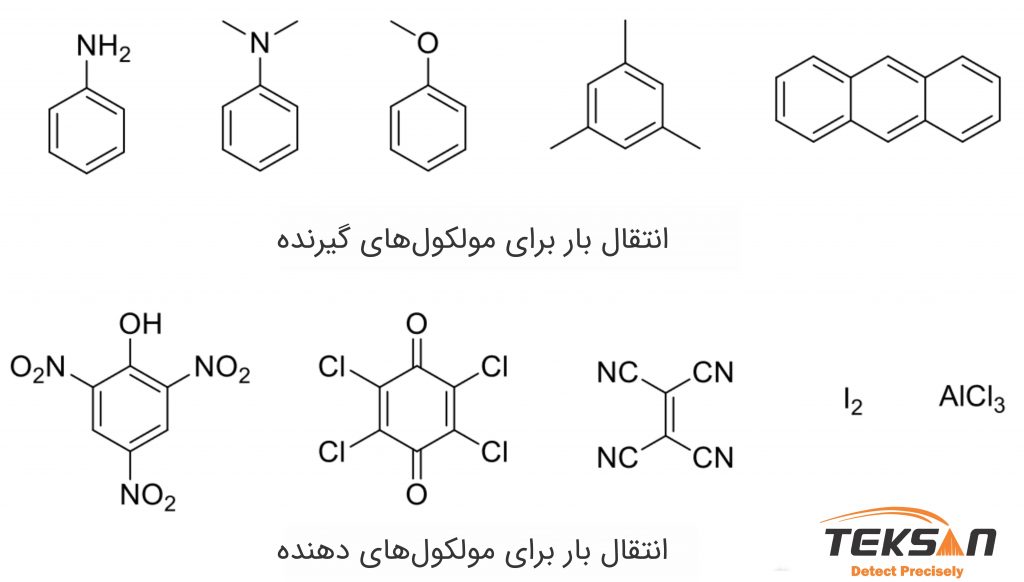
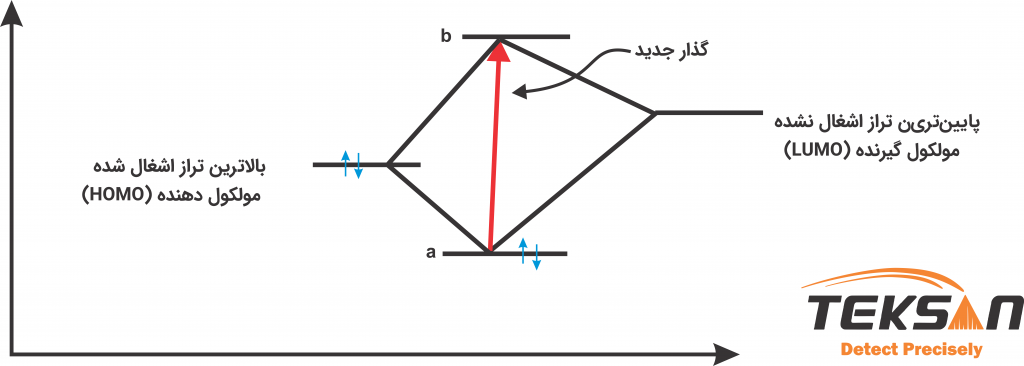
در این مجموعهها اوربیتال π پر شده در مولکول دهنده (donor) با اوربیتال خالی در مولکول پذیرنده (acceptor) همپوشانی دارد. همین همپوشانی اوربیتال سبب میشود تا دو اوربیتال موکلولی جدید ایجاد شود. بنابراین انتقال بین این اوربیتالهای تازه تشکیل شده باندهای جذبی جدیدی در طیف جذبی به وجود میآورند. دو اوربیتال مولکولی تشکیل شده و انتقال بار بین آنها در شکل ۵ نشان داده شده است. به وسیله طیف سنج یووی ویز میتوان این اوربیتالهای ایجاد شده را شناسایی کرد.
رنگ قهوهای ید در بنزن یا رنگ آبی پررنگی که در اثر افزودن تتراسیانو اتیلن به محلول کلروفرم آنیلین به وجود میآید، به دلیل تشکیل مجموعههای انتقال بار است.
توانایی اسپکتروفتومتری در تشخیص پایداری دو شکل توتومری (Tautomer)
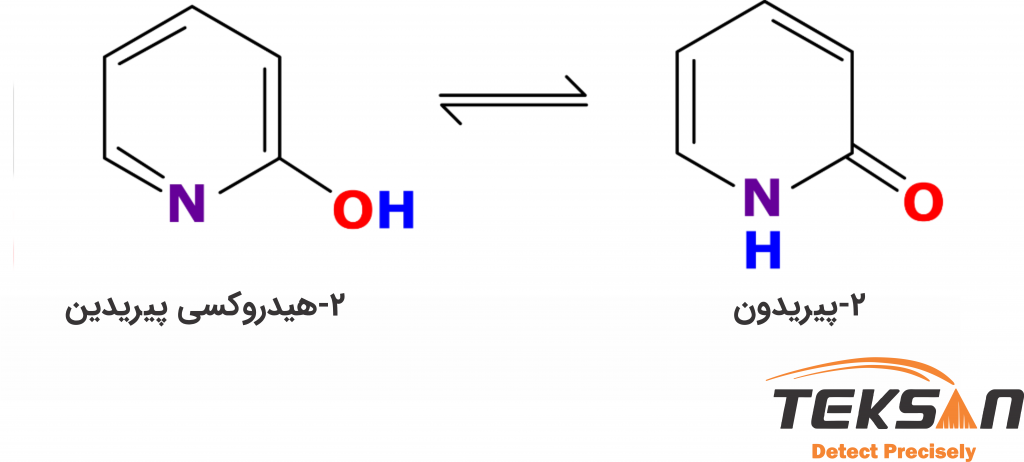
به ترکیبهایی که ساختار آنها از نظر آرایش اتمها متفاوت باشد، توتومر گفته میشود. در هر شرایطی تعادل بین توتومرها به نفع توتومر پایدارتر است. بنابراین تشخیص توتومر پایدار مهم است. به وسیله اسپکتروفتومتر میتوان ترجیح یک ساختار بر ساختار دیگری را تشخیص داد. به عنوان مثال در توتومری ۲-هیدروکسی پیریدین و ۲-پیریدون، دومین ساختار ترجیح داده میشود، زیرا پایدارتر است.
تعیین پیکربندی ایزومرهای هندسی
ایزومری سیس (cis) و ترانس (trans)، که به عنوان ایزومریسم هندسی یا ایزومریسم پیکربندی نیز شناخته میشود، اصطلاحی است که در شیمی آلی به کار میرود. پیشوندهای cis و trans برگرفته از زبان لاتین و به معنی این طرف و طرف دیگر هستند. ایزومز سیس نشان میدهد که گروههای عملکردی در یک طرف هستند. در حالی در ایزومرهای ترانس این گروهها در طرف مقابل هم قرار دارند.
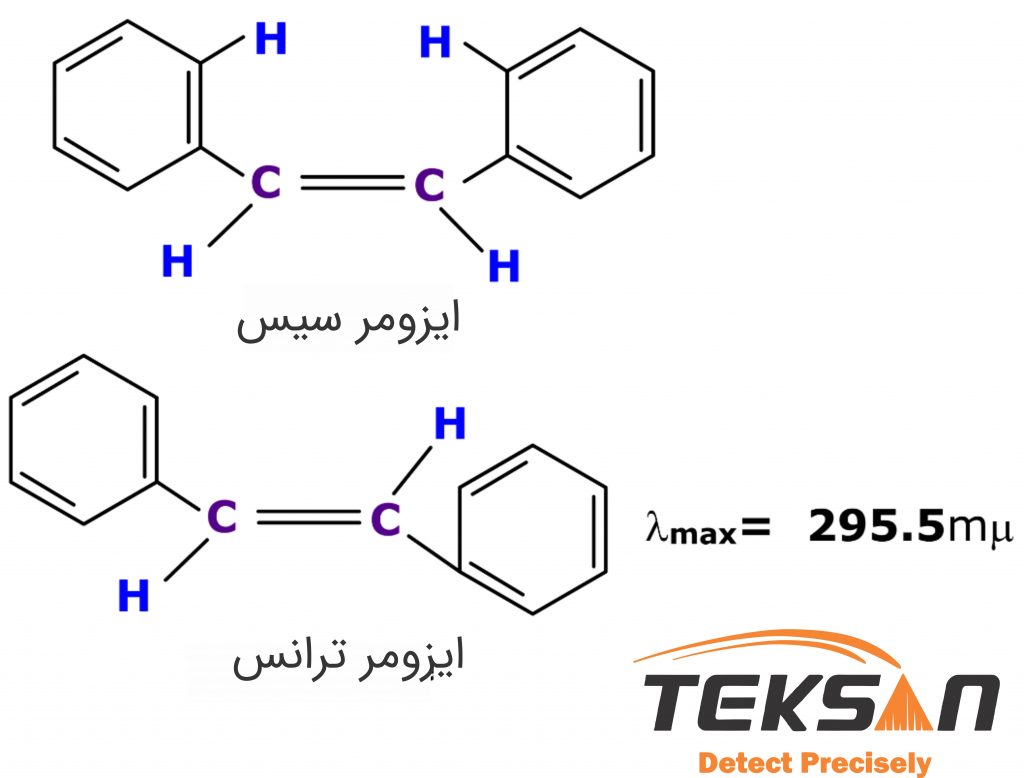
ایزومرهای سیس باتوجه به اعوجاجی که دارند همسطح نیستند. بنابراین نور را در طولموجهای کمتری جذب میکنند. اما ایزومرهای ترانس با توجه به ساختارشان دارای اعوجاج نبوده و نور را در طولموجهای بالاتری جذب میکنند. به این ترتیب با استفاده از طیف جذبی این ایزومرها میتوان پیکربندی آنها را تعیین کرد.
تفکیک ترکیبات همیوغ (conjugated) و غیر همیوغ
طیف سنج مرئی فرابنفش ابزار بسیار خوبی برای تعیین ترکیبات همیوغ و غیر همیوغ است. در این ترکیبات برای باند n به *π برای گروه کربونیل، نور در طولموج بیشتری جذب سیستم خواهد شد. در صورت عدم وجود گروه کربونیل در سیستم، نور برای همان باند در طولموج کوتاهتری جذب سیستم میشود.
تشخیص ساختارهای محوری و استوایی
در برخی از ساختارها اتمهایی که در پیوندهای غیر حلقهای شرکت دارند یا به صورت عمودی قرار میگیرند که در این صورت به آنها ترکیبات محوری گفته میشود و یا به صورت تقریبا افقی قرار دارند که به آنها ساختارهای استوایی گفته میشود. به بیانی دیگر پیوندهای اتمهای غیر حلقهای با زاویه ۹۰ درجه نسبت به صفحه حلقهای، محوری و پیوندها با اتمهای غیر حلقه ای که در مقایسه با صفحه حلقه فقط زاویه کمی ایجاد می کنند استوایی نامیده می شوند. هر یک از این ساختارها طیف جذبی منحصر به فردی دارند. ساختارهای محوری نور را در طولموجهای بلندتری نسبت به ساختارهای استوایی جذب میکنند. بنابراین با در دست داشتن طیف جذب این ساختارها محوری و استوایی بودن آنها را میتوان تعیین کرد.
تعیین وزن مولکولی
وزن مولکولی ترکیبات را میتوان با استفاده از روش اسپکتروفتومتری و آماده سازی مشتقات این ترکیبها اندازهگیری نمود. برای مثال اگر بخواهیم وزن مولکولی آمین را اندازهگیری کنیم، آن را ابتدا به آمین پیکرات (amine picrate) تبدیل میکنیم. سپس غلظت مشخصی از آمین پیکرات را در یک لیتر حلال حل میکنیم و شدت نور را در ۳۸۰ نانومتر اندازهگیری مینماییم. حال میتوان با استفاده از میزان جذب و غلظت، وزن مولکولی را محاسبه کرد.
جمعبندی
با توجه به اهمیت علم شیمی این مقاله را به بررسی کاربرد اسپکتروفتومتری UV-VIS اختصاص دادیم. اسپکتروفتومتری تکنیکی است که در زمینه شیمی به طور گستردهای مورد استفاده قرار میگیرد. کاربردهای این روش شامل تجزیه و تحلیل کمی، تجزیه و تحلیل کیفی، مطالعه مجموعههای انتقال بار، ترجیح دو شکل توتومری، تعیین پیکربندی ایزومرهای هندسی، تفکیک ترکیبات همیوغ و غیر همیوغ، تشخیص ساختارهای محوری و استوایی و تعیین وزن مولکولی است. هر یک از موضوعات را به طور خلاصه بررسی کردیم. همچنین بیان کردیم که به وسیله دستگاه اسپکتروفتومتر چگونه میتوانیم این موارد را مورد مطالعه قرار دهیم.
اگر در مورد مطالب علمی سوالی داشتید میتوانید با مراجعه به قسمت سوالات متداول پاسخ پرسش خود را بیابید.
منابع
- https://zaya.io/doy9s
- https://zaya.io/frwdg
- https://zaya.io/zetfs